Nat Med |Multi-omički pristup mapiranju integriranog tumorskog, imunološkog i mikrobnog pejzaža kolorektalnog karcinoma otkriva interakciju mikrobioma s imunološkim sistemom
Iako su biomarkeri primarnog karcinoma debelog crijeva intenzivno proučavani posljednjih godina, trenutne kliničke smjernice se oslanjaju samo na stadijume tumora-limfnih čvorova-metastaza i otkrivanje defekata popravke neusklađenosti DNK (MMR) ili mikrosatelitne nestabilnosti (MSI) (pored standardnog patološkog testiranja). ) da odredite preporuke za liječenje.Istraživači su primijetili nedostatak povezanosti između imunoloških odgovora zasnovanih na ekspresiji gena, mikrobnih profila i tumorske strome u kohorti raka debelog crijeva Atlas genoma raka (TCGA) i preživljavanja pacijenata.
Kako je istraživanje napredovalo, prijavljeno je da kvantitativne karakteristike primarnog kolorektalnog karcinoma, uključujući ćelijsku, imunološku, stromalnu ili mikrobnu prirodu raka, značajno koreliraju s kliničkim ishodima, ali još uvijek postoji ograničeno razumijevanje o tome kako njihove interakcije utječu na ishode pacijenata. .
Da bi secirao odnos između fenotipske složenosti i ishoda, tim istraživača sa Instituta za medicinska istraživanja Sidra u Kataru nedavno je razvio i potvrdio integrirani rezultat (mICRoScore) koji identificira grupu pacijenata s dobrim stopama preživljavanja kombinacijom karakteristika mikrobioma i imunološkog odbacivanja. konstante (ICR).Tim je izvršio sveobuhvatnu genomsku analizu svježe smrznutih uzoraka od 348 pacijenata s primarnim kolorektalnim karcinomom, uključujući sekvenciranje RNA tumora i odgovarajućeg zdravog kolorektalnog tkiva, sekvenciranje cijelog egzoma, duboki T-ćelijski receptor i sekvenciranje gena 16S bakterijske rRNA, dopunjeno cijelim tumorom. sekvenciranje genoma za daljnju karakterizaciju mikrobioma.Studija je objavljena u Nature Medicine kao “Integrirani tumor, imunološki i mikrobiomski atlas raka debelog crijeva”.

Članak objavljen u Nature Medicine
AC-ICAM pregled
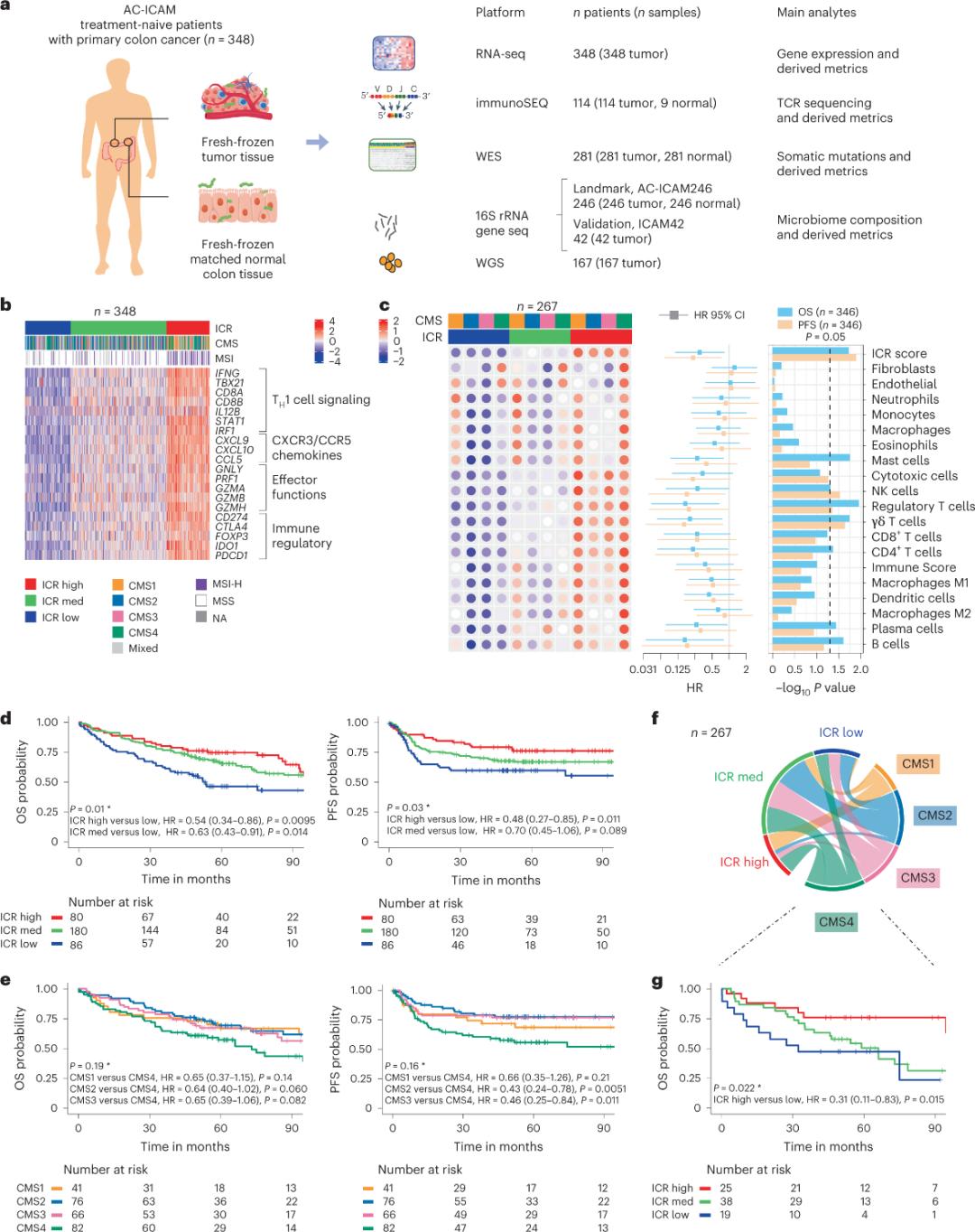
Istraživači su koristili ortogonalnu genomsku platformu kako bi analizirali svježe smrznute uzorke tumora i uparili susjedno zdravo tkivo debelog crijeva (tumor-normalni parovi) od pacijenata sa histološkom dijagnozom raka debelog crijeva bez sistemske terapije.Na osnovu sekvenciranja cijelog egzoma (WES), kontrole kvaliteta podataka RNA-seq i skrininga kriterija uključivanja, genomski podaci od 348 pacijenata su zadržani i korišteni za nizvodnu analizu s medijanom praćenja od 4,6 godina.Istraživački tim je ovaj resurs nazvao Sidra-LUMC AC-ICAM: mapa i vodič za interakcije imunog raka-mikrobioma (Slika 1).
Molekularna klasifikacija korištenjem ICR
Snimajući modularni skup imunoloških genetskih markera za kontinuirani imunonadzor raka, nazvan imunološka konstanta odbacivanja (ICR), istraživački tim je optimizirao ICR kondenzirajući ga u panel od 20 gena koji pokriva različite tipove raka, uključujući melanom, rak mokraćne bešike i rak dojke.ICR je također povezan s imunoterapijskim odgovorom kod različitih tipova raka, uključujući rak dojke.
Prvo, istraživači su potvrdili ICR potpis AC-ICAM kohorte, koristeći pristup koklasifikacije zasnovan na ICR genima da klasifikuju kohortu u tri klastera/imuni podtipa: visok ICR (vrući tumori), srednji ICR i nizak ICR (hladni tumori) (Slika 1b).Istraživači su okarakterizirali imunološku sklonost povezanu s konsenzusnim molekularnim podtipovima (CMS), klasifikacijom raka debelog crijeva zasnovanom na transkriptomima.CMS kategorije su uključivale CMS1/imuni, CMS2/kanonski, CMS3/metabolički i CMS4/mezenhimski.Analiza je pokazala da su ICR rezultati u negativnoj korelaciji sa određenim putevima ćelija raka u svim CMS podtipovima, a pozitivne korelacije sa imunosupresivnim i stromalnim putevima uočene su samo kod CMS4 tumora.
U svim CMS-om, broj podskupova ćelija prirodnih ubica (NK) i T ćelija bio je najveći u podtipovima visokog imuniteta ICR, sa većom varijabilnosti u drugim podskupovima leukocita (Slika 1c). ICR imuni podtipovi su imali različite OS i PFS, sa progresivnim povećanjem u ICR-u od niskog do visokog (Slika 1d), potvrđujući prognostičku ulogu ICR-a u kolorektalnom karcinomu.
Slika 1. Dizajn AC-ICAM studije, imuno-povezani genski potpis, imunološki i molekularni podtipovi i preživljavanje.
ICR hvata tumorom obogaćene, klonalno amplificirane T ćelije
Prijavljeno je da je samo manjina T ćelija koje infiltriraju tumorsko tkivo specifična za tumorske antigene (manje od 10%).Stoga se većina intratumorskih T ćelija naziva T-ćelijama posmatrača (bystander T ćelije).Najjača korelacija sa brojem konvencionalnih T ćelija sa produktivnim TCR uočena je u subpopulacijama stromalnih ćelija i leukocita (detektovanih pomoću RNA-seq), koje se mogu koristiti za procenu subpopulacija T ćelija (Slika 2a).U ICR klasterima (ukupna i CMS klasifikacija), najveća klonalnost imunih SEQ TCR-ova primijećena je u grupama ICR-high i CMS podtipa CMS1/imunih grupa (Slika 2c), s najvećim udjelom tumora sa visokim ICR-om.Koristeći cijeli transkriptom (18.270 gena), šest ICR gena (IFNG, STAT1, IRF1, CCL5, GZMA i CXCL10) bili su među prvih deset gena koji su pozitivno povezani sa TCR imunim SEQ klonalnošću (Slika 2d).ImmunoSEQ TCR klonalnost je jače korelirala sa većinom ICR gena nego korelacije uočene korišćenjem CD8+ markera koji reaguju na tumor (Slike 2f i 2g).U zaključku, gornja analiza sugerira da ICR potpis bilježi prisustvo tumorom obogaćenih, klonalno amplificiranih T ćelija i može objasniti njegove prognostičke implikacije.
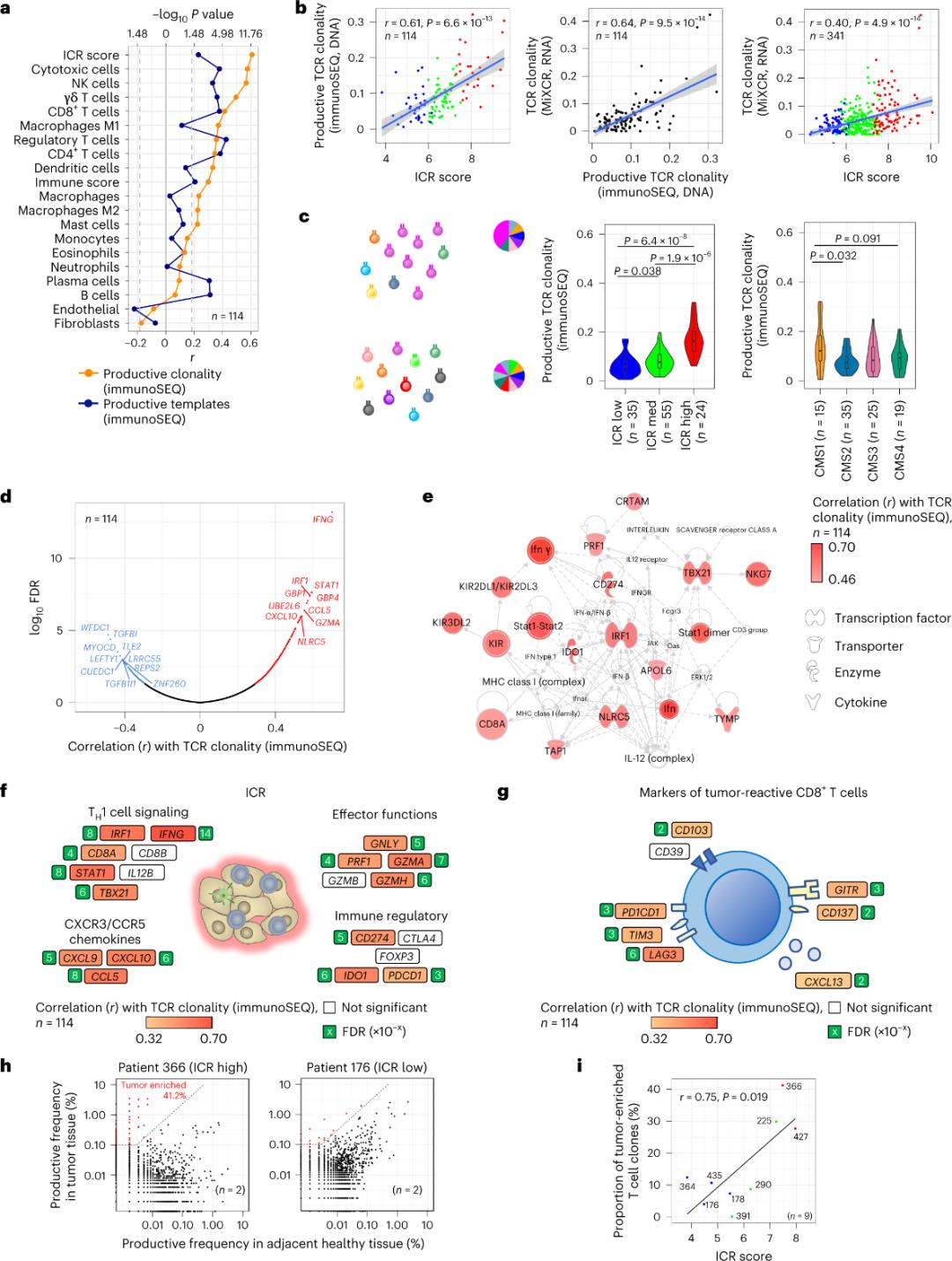
Slika 2. TCR metrika i korelacija sa genima vezanim za imunitet, imunološkim i molekularnim podtipovima.
Sastav mikrobioma u zdravom tkivu i tkivu raka debelog crijeva
Istraživači su izvršili sekvenciranje 16S rRNA koristeći DNK ekstrahiranu iz podudarnog tumora i zdravog tkiva debelog crijeva od 246 pacijenata (slika 3a).Za provjeru valjanosti, istraživači su dodatno analizirali podatke sekvenciranja gena 16S rRNA iz dodatna 42 uzorka tumora koji nisu odgovarali normalnom DNK dostupnom za analizu.Prvo, istraživači su uporedili relativnu količinu flore između podudarnih tumora i zdravog tkiva debelog crijeva.Clostridium perfringens je značajno povećan u tumorima u poređenju sa zdravim uzorcima (Slika 3a-3d).Nije bilo značajne razlike u alfa raznolikosti (raznolikost i brojnost vrsta u jednom uzorku) između tumorskih i zdravih uzoraka, a uočeno je skromno smanjenje mikrobne raznolikosti kod tumora sa visokim ICR u odnosu na tumore sa niskim ICR.
Kako bi otkrili klinički relevantne veze između profila mikroba i kliničkih ishoda, istraživači su imali za cilj koristiti podatke sekvenciranja gena 16S rRNA kako bi identificirali karakteristike mikrobioma koje predviđaju preživljavanje.Na AC-ICAM246, istraživači su pokrenuli OS Cox regresijski model koji je odabrao 41 karakteristiku s koeficijentima koji nisu nula (povezani s diferencijalnim rizikom smrtnosti), nazvanim MBR klasifikatorima (slika 3f).
U ovoj kohorti obuke (ICAM246), nizak MBR skor (MBR<0, nizak MBR) bio je povezan sa značajno nižim rizikom od smrti (85%).Istraživači su potvrdili povezanost između niskog MBR (rizika) i produženog OS u dvije nezavisno validirane kohorte (ICAM42 i TCGA-COAD).(Slika 3) Studija je pokazala snažnu korelaciju između endogastričnih koka i MBR rezultata, koji su bili slični u tumoru i zdravom tkivu debelog crijeva.
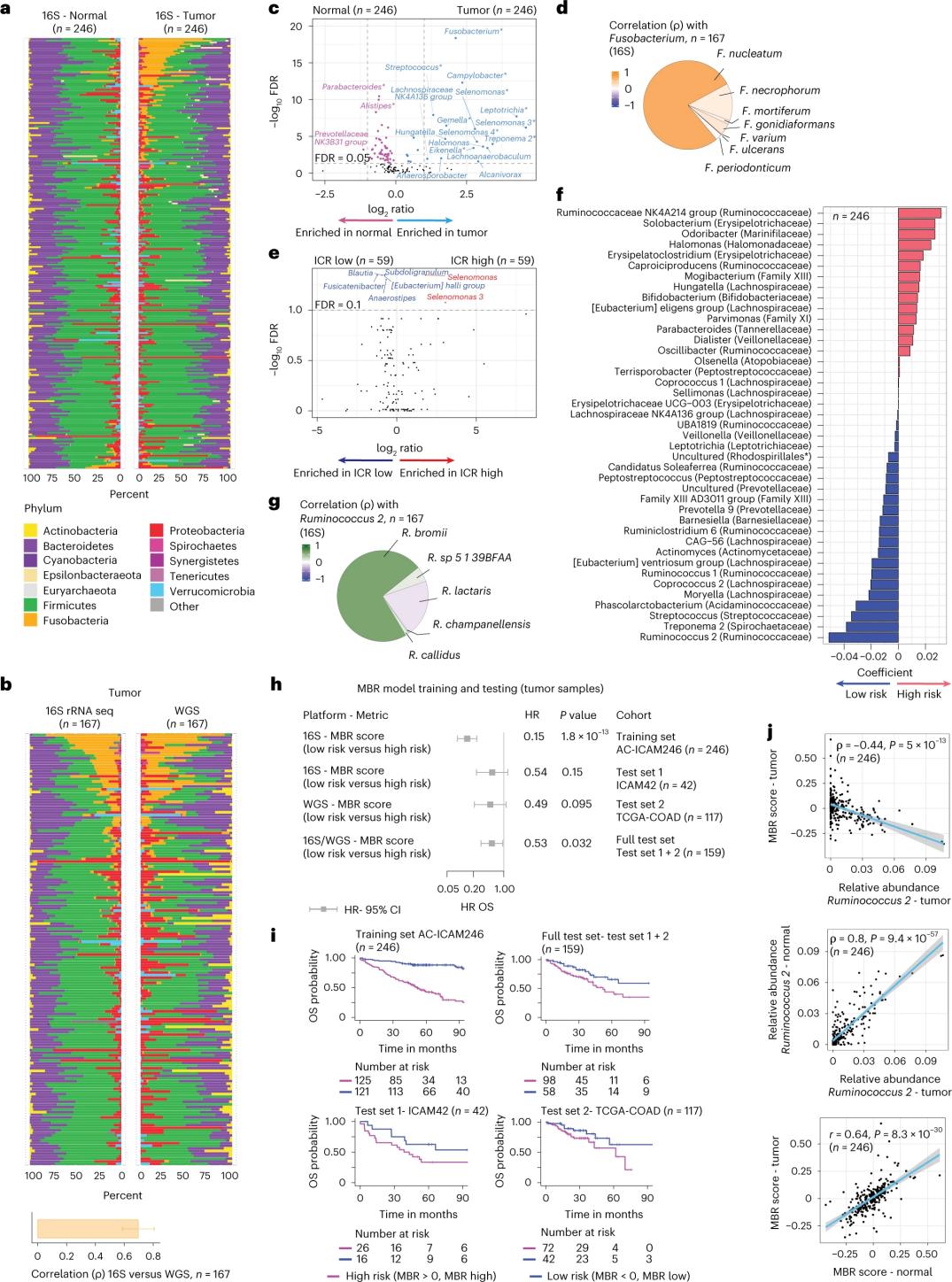
Slika 3. Mikrobiom u tumoru i zdravim tkivima i odnos sa ICR-om i preživljavanjem pacijenata.
Zaključak
Multi-omički pristup korišćen u ovoj studiji omogućava temeljnu detekciju i analizu molekularnog potpisa imunog odgovora kod kolorektalnog karcinoma i otkriva interakciju između mikrobioma i imunog sistema.Duboko TCR sekvenciranje tumora i zdravih tkiva otkrilo je da prognostički učinak ICR-a može biti posljedica njegove sposobnosti da uhvati tumorom obogaćene i možda tumorski antigen-specifične klonove T stanica.
Analizom sastava tumorskog mikrobioma koristeći sekvenciranje gena 16S rRNA u AC-ICAM uzorcima, tim je identificirao mikrobiomski potpis (MBR skor rizika) sa jakom prognostičkom vrijednošću.Iako je ovaj potpis izveden iz uzoraka tumora, postojala je jaka korelacija između zdravog kolorektuma i tumorskog MBR rezultata, što sugerira da ovaj potpis može obuhvatiti sastav crijevnog mikrobioma pacijenata.Kombinacijom ICR i MBR rezultata, bilo je moguće identificirati i potvrditi multi-omični student biomarker koji predviđa preživljavanje kod pacijenata s rakom debelog crijeva.Multi-omični skup podataka studije pruža resurs za bolje razumijevanje biologije raka debelog crijeva i pomaže u otkrivanju personaliziranih terapijskih pristupa.
Vrijeme objave: Jun-15-2023
 中文网站
中文网站